| 5. A Természetes koncentrációcsökkenési folyamatok monitoringja | |||
| 5.1 A természetes koncentrációcsökkenési folyamatok szerepe, működése | |||
A természetes koncentrációcsökkenés a természetben előforduló folyamatoknak köszönhető szennyezőanyag komponensek koncentrációjában, tömegében vagy mobilitásában beállt csökkenés, amely függ a távolságtól és az időtől. Ezek a folyamatok lehetnek fizikai (diszperzió, diffúzió, hígulás, kipárolgás), kémiai (megkötődés, kémiai vagy abiotikus reakciók) vagy biológiai (biodegradáció) folyamatok. A természetes koncentrációcsökkenés a környezeti koncentráció kialakulásában játszik szerepet.
A szennyezőanyagok terjedési útvonalán bekövetkező koncentrációcsökkenését a koncentrációcsökkenési állandó (Natural Attenuation Factor=NAF) becslésével lehet figyelembe venni. A fizikai és kémiai folyamatok csökkentik a szennyezőanyag koncentrációját és/vagy mobilitását, de nem csökkentik a szennyezőanyag mennyiségét (nem destruktív folyamatok). A kémiai és biológiai reakciók viszont lecsökkentik a szennyezőanyag abszolút mennyiségét (destruktív folyamatok). Az egyes folyamatok hatását a szennyezőanyag koncentrációra az 5.1-1. ábra mutatja be. Mivel számos koncentrációcsökkentő folyamat reverzibilis (beoldódás-kicsapódás), bizonyos esetekben figyelembe kell venni a szennyezőanyag koncentrációját növelő folyamatokat is. Ilyen folyamatok a sav-bázis reakciók, a koszolvencia, kicsapódás, deszorbció, komplexek megbomlása, stb.
5.1-1. ábra
A szennyezőanyag koncentrációjának változása koncentrációcsökkentő folyamatok hatására
Forrás: USEPA, 1991.
A főbb szennyező vegyi anyag csoportokra vonatkozó destruktív, illetve nem destruktív koncentrációcsökkentő folyamatokat az 5.1-1. táblázat mutatja be összefoglalóan, míg a szennyezőanyagok terjedését befolyásoló fontosabb folyamatokat és azok jellemzőit az 5.1-2. táblázat foglalja össze.
5.1-1. táblázat
Az egyes vegyi anyagokra jellemző koncentráció-csökkentő folyamatok
|
Nem-destruktív koncentráció-csökkentő folyamatok 1 |
Destruktív (degradatív) koncentrációcsökkentő folyamatok 2 | ||||||||||
|
Metileződés |
Kicsapódás 3 és kation csere |
Szorpció 4 |
Párolgás 5 |
Aerob degradáció (a szennyező-anyag mint elektron donor) 6 |
Anaerob degradáció (a szennyező-anyag mint elektron donor) 7 |
Reduktív deklorináció (a szennyezőanyag mint elektron akceptor) |
Fermentáció |
Kometabolizmus |
Oxidáció/redukció | ||
|
Szennyezőanyag típusa |
Például | ||||||||||
|
Klórozott szénhidrogének 8,9 3 vagy több klór atom |
PCE, TCE, TCA |
x |
x |
x? |
x |
xx |
x |
x | |||
|
Klórozott szénhidrogének 8,9 3-nál kevesebb klór atom |
DCM, VC, DCE |
x |
x |
xx |
x |
x 10 |
x | ||||
|
Petróleum szénhidrogének |
BTEX, fehéráruk |
x |
x |
xx |
x |
x |
x | ||||
|
Oxigenátok |
MTBE, TAME |
x |
xx |
x | |||||||
|
Nehézfémek (kationos) |
Hg, Cd, Zn, Pb, Ni, Sr, Co |
x 11 |
x |
xx | |||||||
|
Nehézfémek (anionos) |
CrO4AsO4 AsO3TcO4 |
xx | |||||||||
|
Szervetlen vegyületek |
Ca, Mg, Si |
xx | |||||||||
|
Anionok |
PO4, BO3 |
xx |
xx | ||||||||
|
Amónia |
NH3NH4 |
xx |
x |
x | |||||||
|
Cianid |
CN |
x |
x |
x | |||||||
|
Nitrát |
NO3 |
x |
x |
xx | |||||||
|
PAH-ok |
Naftalin |
xx |
x |
x |
x? | ||||||
|
Krezolok |
Fenol |
x |
xx |
xx |
x |
x | |||||
|
Peszticidek 12 |
x |
x |
x |
x? |
x? | ||||||
xx = elsődleges fontosságú, x = másodlagos jelentőségű, ? = bizonytalan a folyamat jelentősége
- A szervetlen szennyezőanyagok mobilitásának, toxikusságának valamint biológiai hozzáférhetőségének csökkenését jellemzően a szorpció és redox reakciók okozzák. A csapadékképződéssel járó reakciók és a talaj pórusterében történő megkötődés általában irreverzibilis folyamatok, míg a felületi adszorpció és a komplex-képződés okozta koncentrációcsökkenések reverzibilisek. A szennyezőanyag koncentráció, a pH és a redox potenciál változása következtében a korábban immobil, kötött formájú szennyezőanyagok felszabadulhatnak.
- Szerves és szervetlen szennyezőanyagok (pl. ammónia) mennyisége a fémek kivételével olyan (bio)kémiai reakciókkal is csökkenthető, mint a hidrolízis (reakció a vízzel, savakkal-lúgokkal), fotolízis (reakció a napfénnyel, vagy fényenergia által termelt reaktív gyökökkel), biodegradáció (reakció enzimekkel vagy egyéb biogén anyagokkal), oxidáció (reakció az oxigénnel), reduktív/eliminatív folyamatok. Általában az abiotikus folyamatok lassabbak mint a biodegradáció, de egy jellemző kivétel az 1,1,1-TCA lebomlása. Sok szerves szennyezőanyag viselkedését, terjedését elsősorban a biodegradáció határozza meg. Az oldott szennyezőanyagok, mint például a triklór-metán egy sor oxidációs-redukciós reakció után olyan ártalmatlan melléktermékké átalakul át, mint a széndioxid, klorid, metán és a víz. Bár a biodegradáció során olyan közbülső termékek is képződhetnek, melyek sokkal toxikusabbak, mobilisabbak, mint a kiindulási vegyület. Az alábbi biodegradációs folyamatok ismertek:
- aerob degradáció – szerves vegyületek átalakítása/eliminációja mikroorganizmusok által oxigén jelenlétében. Termodinamikailag gyakran ez a legkedvezőbb folyamat;
- anaerob degradáció – szerves vegyületek átalakítása és/vagy eliminációja mikroorganizmusok által oxigén hiányában. Elektron akceptorként léphet föl pl.: a nitrát, mangán (IV), vas (III), szulfát és szén-dioxid;
- halorespiráció – a halogén tartalmú szennyezőanyag nem szénforrásként, hanem elektron akceptorként vesz részt a biodegradációs folyamatban, ahol a klór (halogén) atomok hidrogénre cserélődnek ki, és a szerves vegyületek fermentációjából származó hidrogén elektron donorként viselkedik.
- fermentáció – elektron átmenettel (cserével) járó redox reakciók szerves vegyületek között;
- kometabolizmus – a szerves szennyezőanyagok olyan degradációja, amikor mikroorganizmusok által – nem a degradáció miatt, hanem más célból termelt enzimek vagy kofaktorok katalizálják a szennyezőanyag bomlását, de a mikroorganizmusoknak nem származik előnye a szennyezőanyagok bomlásából. A szennyezőanyagok indirekt biodegradációja során a mikroorganizmusok BTEX-et vagy egyéb szubsztrátot használnak föl szénforrásként energiaigényük fedezésére. A többszörösen klórozott alifás komponensek (PCE és TCE) biodegradációjának gyakori módja az anaerob kometabolizmus (”reduktív deklorináció”). A reduktív deklorináció már nitrát-/szulfátredukáló körülmények között is folyik, de a legnagyobb degradációs sebesség metanogén körülmények között alakul ki.
3. Például kicsapódás oldhatatlan szulfid és karbonát formában.
4. Például szorpció vas-hidroxidra, karbonátokra, agyagásványokra.
5. Elsődlegesen a telítettlen zónában.
6. Aerob degradáció – oxigén mint elektron akceptor.
7. Anaerob degradáció – denitrifikáció, Fe(III) redukció, szulfát redukció, metanogenezis, ahol a NO3, Fe, SO4, és CO2(ebben a sorrendben) és a klórozott oldószerek mint elektron akceptorok vesznek részt a folyamatban. A klórozott szénhidrogének közül csak a VC és DCM képes anaerob körülmények között elsődleges szubsztrátként (elektron donorként) viselkedni.
8. PCE = tetraklór-etilén; TCE = triklór-etilén; TCA = 1,1,1-triklór-etán; TCM = triklór-metán; DCM = diklór-metán; VC = vinil-klorid; DCE = diklór-etilén
9. Többszörösen halogénezett szénhirdogének aerob úton nem degradálódnak.
10. A DCM lehetséges, hogy degradálódik fermentáció útján.
11. A higanyt metileződhet, és a keletkezett metil-higany, amely elpárolog.
12. pl.:lindán, malation, triazin.
5.1-2. táblázat
A szennyezőanyagok terjedését befolyásoló fontosabb folyamatok
|
Folyamat |
Leírás |
Amitől függ |
Hatás |
|
Advektív transzport |
Az oldott anyag mozgása a talajvíz mozgásával |
Függ a víztartó réteg tulajdonságaitól, főleg a szivárgási tényezőtől, az effektív porozitástól valamint a hidraulikus gradienstől. Független a szennyezőanyag tulajdonságaitól |
A fő mechanizmus, ami a szennyezőanyagok terjedését előidézi a felszín alatt. |
|
Diszperzió |
Keveredés a talajvíz áramlása és a víztartó réteg egyenetlenségei miatt. |
Függ a víztartó réteg tulajdonságaitól, de független a szennyezőanyag tulajdonságaitól. |
A csóvának hosszanti, keresztirányú és függőleges növekedését idézi elő. Csökkenti az oldott szennyezőanyag koncentrációját. |
|
Diffúzió |
A molekuláris diffúzió miatt a szennyezőanyag szétterjed és felhígul. |
Függ a szennyezőanyag tulajdonságaitól, valamint a koncentráció gradienstől. A Fick- törvény írja le. |
A szennyezőanyagok diffúziója a magasabb koncentrációjú helyekről a kisebb koncentrációjú helyek felé. Elhanyagolható a diszperzióhoz képest majdnem minden talajvíz áramlási sebesség esetén. |
|
Szorpció |
Reakció a víztartó közeg és az oldott anyag között, amikor a szennyezőanyagok abszorbálódnak a szerves szén-tartalomra vagy agyagásványokra. |
Függ a víztartó közeg tulajdonságaitól (szerves szén és agyagásvány tartalom, sűrűség, fajlagos felület, porozitás) és a szennyezőanyag tulajdonságaitól (oldhatóság, hidrofobicitás, oktanol-víz megoszlási hajlam) |
Az oldott anyag áramlási sebességét lecsökkenti a víz szivárgási sebességéhez képest, és kivonja az oldatból a szennyezőanyag egy részét. |
|
Beszivárgás (egyszerű hígulás) |
Víz mozgása a telítetlen zónán keresztül a vízszintig. |
Függ a víztartó réteg tulajdonságaitól, a talajvíz mélységétől, a felszíni víz-felszín alatti víz kölcsönhatástól, és az éghajlattól |
A szennyezőanyag hígulását okozza és utánpótlását képzi az oldott oxigénnek. |
|
Párolgás |
A talajvízben oldott szennyezőanyagok párolgása gőz fázisba (talaj gáz) |
Függ a vegyi anyagok parciális nyomásától, és a Henry állandótól. |
A szennyezőanyagot oldott fázisból eltávolítja, és a talajgázba juttatja. |
|
Biodegradáció |
Mikrobiológiai úton lezajló redox reakció, melyben a szennyezőanyag lebomlik. |
A felszín alatti víz geokémiájától, mikróba populációtól és a szennyezőanyag tulajdonságaitól függ. A biodegradáció lejátszódhat aerob és/vagy anaerob úton. |
A szennyezőanyag teljes degradációját eredményezheti. A legfontosabb a szerves szennyezőanyagok koncentrációcsökkentő folyamatai között. |
|
Abiotikus degradáció |
Olyan kémiai átalakulások, mint pl. a hidrolízis, amely degradálja a szennyezőanyagot mikrobiológiai segítség nélkül. |
A szennyezőanyag tulajdonságaitól és a talajvíz geokémiájától függ. |
A szennyezőanyag teljes vagy részleges lebomlásához vezethet. Sokkal lassabb folyamatok, mint a biodegradáció. |
|
NAPL megoszlása |
NAPL beszivárgása a talajvízbe és megkötődése a talajszemcséken. Az NAPL csóvák mobil és reziduális fázisban folyamatos utánpótlódási forrásként viselkednek. |
Függ a víztartó réteg és a szennyezőanyag tulajdonságaitól, az NAPL csóván keresztül haladó és a csóva mögötti területen kialakuló talajvíz fluxustól. |
A szennyezőanyagok beoldódása az NAPL-ből az elsődleges forrásai a talajvízben oldott szennyeződésnek. |
| 5.2 Fizikai koncentrációcsökkentő folyamatok | |||
A legfontosabb fizikai koncentrációcsökkentő folyamatok a hidrodinamikus diszperzió (diffúzió és mechanikai diszperzió), a hígulás és a kipárolgás.
A párolgás kivételével ezek a folyamatok szinte minden oldott anyag koncentrációját befolyásolják. A párolgás a szervetlen szennyezőanyagokra – kevés kivétellel – nem jellemző, de a többi pusztán fizikai koncentrációcsökkentő folyamat hatással van az oldott szervetlen anyagokra is, így ebben a fejezetben a szervetlen és szerves vegyi anyagokra jellemző folyamatok szétválasztása nem indokolt.
| 5.2.1. Mechanikai diszperzió | |||
A mechanikai diszperzió során a vegyi anyagok szétterjednek az advektív mozgás és a közvetítő közeggel való kölcsönhatás miatt. Ennek két komponense van:
- longitudinális diszperzió (a felszín alatti vízmozgás irányában) és
- transzverzális diszperzió (a felszín alatti vízmozgás irányára merőlegesen).
Longitudinális diszperziót okoz a pórusméret megváltozása, a zegzugos áramlási pálya és a pórusokbeli súrlódás. A transzverzális diszperziót a porózus közeg zegzugos pórustere eredményezi, amely a csóva középvonalára merőleges irányú szétterjedést okozza (5.2.1-1. ábra). Általában a mechanikai diszperzió felelős a hidrodinamikai diszperzióért.
5.2.1-1. ábra
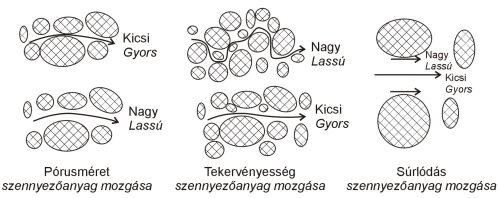

A mechanikai diszperzió kialakulásának okai

Forrás: USEPA, 1991.
| 5.2.2 Molekuláris diffúzió | |||
A molekuláris diffúzió egy vegyi anyagnak a kisebb koncentrációjú hely felé történő mozgása. Felszín alatti vízben ez a mozgás akár vízáramlás hiányában is kialakul. Az oldott szennyezőanyagok molekuláris diffúzióját a Fick törvény írja le. A szennyezőanyagok vízbeli diffuzivitása a szennyezőanyag molekula átmérőjének, a víz viszkozitásának és a hőmérsékletnek a függvénye.
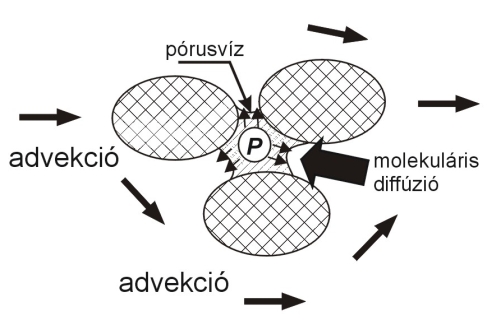
Ez a koncentrációcsökkenési folyamat advektív terjedés esetén elhanyagolható, mert mértéke általában jelentéktelen a mechanikai diszperzióhoz képest, de számottevő lehet áramlásmentes vagy nagyon csekély áramlású közeg esetén (5.2.2-1. ábra).
5.2.2-1. ábra
A molekuláris diffúzió

Forrás: USEPA, 1991.
A hidrodinamikai diszperzió eredményeként tehát a szennyezőanyag csóva szétterjed és keveredik a felszín alatti vízzel. Felszín alatti vizek esetében a hígulás hatásához hozzáadódva a diszperzió elősegítheti a szerves alkotók biodegradációját is, mert a szennyezettség olyan helyekre is eljuthat, ahol több elektron-akceptor vagy -donor található.
| 5.2.3 Hígulás | |||
A hígulás a szennyezetlen felszíni vagy felszín alatti vízzel, valamint a csapadékkal történő keveredést jelenti. További természetes koncentrációcsökkentő hatása a hígulásnak, hogy oldott oxigénben vagy egyéb elektron akceptorban (vagy donorban) gazdag vízzel látja el a szennyezett területet, ezáltal megnövelheti bizonyos szerves szennyezőanyagok biodegradációjának mértékét. Hasonló jelenség figyelhető meg a vízszint szezonális ingadozása következtében csapdázódott oldott oxigén esetén is.
| 5.2.4 Párolgás | |||
Az illékony vegyületek mennyisége lecsökkenhet a felszín alatti környezetből az atmoszférába történő kilépéssel is. Ez a kipárolgás általában két lépésből áll:
1.) a szennyezőanyag kilépése az érintett közegből (talaj, talajvíz) a talajgázba,
2.) a szennyezőanyagok kilépése a talajgázból a légkörbe.
A párolgás mértéke, vagyis a szennyezőanyag ilyen módon történő fogyása függ a vegyi anyag bizonyos tulajdonságától (Henry állandó, diffúziós állandó), a szennyeződést tároló közegtől, a klímától, talajvízmélységtől, adszorpciótól, hőmérséklettől, effektív porozitástól és a talajtípustól.
A Henry-törvény az oldott anyagoknak a talajvízből a talajgázba történő kipárolgási arányát írja le:
|
Ca= H × Cgw |
(1.) |
ahol:
H = Henry állandó (-) vagy (cm 3 /cm 3 )
Ca= levegőbeli koncentráció (g/cm 3 - gőz)
Cgw= vízfázisbeli koncentráció (g/cm 3 - víz)
| 5.3 A szerves vegyületeket jellemző kémiai koncentrációcsökkentő folyamatok | |||
A 5.1-1. táblázat alapján látható, hogy a szerves és szervetlen szennyezőanyagok előre jelezhető koncentrációit – eltérő kémiai formáik és viselkedésük miatt – eltérő kémiai koncentrációcsökkentő folyamatok figyelembe vételével lehet becsülni. Ezért különválasztva tárgyalja az útmutató a szerves és szervetlen szennyezőanyagokra jellemző kémiai folyamatokat.
| 5.3.1 Szorpció (megkötődés) | |||
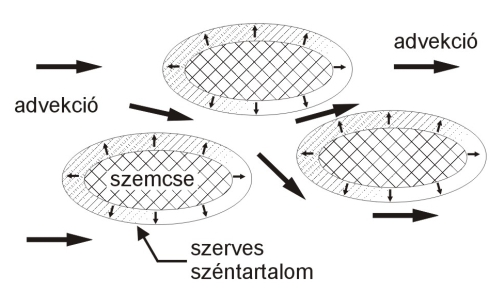
A vegyi anyagok terjedése a felszín alatti vízben jelentősen függ a szorpció mértékétől. A szorpció mértékét pedig jelentősen befolyásolja a szilárd fázis (talaj, üledék) és a víz fázisai közötti megoszlás, a kipárolgás mértéke és a vegyi anyagok biológiai hozzáférhetősége. A szorpció a talajvíz szivárgási sebességéhez képest lecsökkenti a hidrofób vegyületek terjedési sebességét és lecsökkenti az oldott koncentrációt a talajvízben, de ez általában a magasabb koncentráció kialakulását okozza a talajban (5.3.1-1. ábra). Tehát ez a folyamat nem jelenti a szennyezőanyag mennyiségének csökkenését, csak az alkotó mobilitásának és koncentrációjának változását. Az oldott vegyi anyag szilárd fázishoz való kötődése tehát reverzibilis folyamat, de a deszorpció általában lassabb, mint a megkötődés.
5.3.1-1. ábra
A szorpció

Forrás: USEPA, 1991.
A szilárd fázisok eltérő szorpciós kapacitásáért az ásványi- és szerves anyag tartalom, a víz, a levegő és a (mikro)organizmusok különböző arányainak köszönhető heterogén talajkémiai és -fizikai viszonyok felelősek. A szorpciót befolyásoló paraméterek között található a szerves széntartalom, szervetlen kolloidtartalom, az agyagtartalom, a pH érték, a nedvességtartalom, a kation-cserélő képesség, a hőmérséklet, stb. A legtöbb víztartóban a szorpciót elsősorban a szerves anyag tartalom, másodsorban az agyagásvány-tartalom szabályozza. A talaj és a földtani közeg összetételének megfelelően szorpciós kapacitásuk is eltérő, tehát ugyanazon vegyi anyag adszorpciós koefficiense több nagyságrendnyi tartományt is felölelhet. A szorpciós izotermák a vegyi anyag talajhoz kötött és a talajjal kapcsolatban lévő oldatban visszamaradó koncentrációjának arányát írják le. Több vegyi anyag szorpcióját jóval nehezebb becsülni, mint az egyedi vegyületekét.
A legtöbb szerves vegyi anyag szorpciója – a legáltalánosabban használt és a legegyszerűbb – lineáris egyensúlyi szorpcióval jól közelíthető.
A megoszlási hányados értéke, Kd, a szorpciós izoterma meredeksége:
|
Kd= Cs/Cgw |
(2.) |
ahol:
Kd= megoszlási hányados (cm 3 /g)
Cs= szorbeált szennyezőanyag koncentráció (g/g-talaj) és
Cgw= oldott szennyezőanyag koncentráció (g/cm 3 -oldat)
A talaj-víz megoszlási hányados, Kdértéke tehát kifejezhető a talajszemcsékre szorbeálódott és az oldatban lévő szennyezőanyag koncentrációjának arányaként. Kdértéke azonban korántsem konstans, értékét igen sok tényező befolyásolja. Ilyen tényezők a víztartó réteg szemcséinek mérete és felülete, a talajvíz összetétele, pH és EH, a vizsgált szennyezőanyag koncentrációja, a hőmérséklet és a nyomás, a víztartó ásványi összetétele, stb. Általában Kdértéke azonban növekszik a talaj szerves anyag tartalmának (foc) növekedésével (Karickhoff, 1981). Másrészről pedig a nem ionos, apoláris hidrofób szerves vegyi anyagoknak a talaj szerves anyag tartalmához való kötődési arányát is egy egyensúlyi folyamattal lehet leírni:
|
Kd= Koc× foc. |
(3.) |
ahol:
Koc[cm 3 /g] a szerves szén megoszlási hányados, amely az focés Kdértékek függvényében felvett egyenes meredeksége, vagyis az adott vegyi anyag szerves-(anyag)szén tartalomhoz való kötődési arányát írja le (5.3.1-2. ábra).
5.3.1-2. ábra
A megoszlási hányados értékének változása a talaj szerves széntartalmának függvényében

Forrás: USEPA, 1991.
A felszín alatti környezetben végbemenő szorpcióból eredő retardáció (R) mértékének közelítésére a következő empirikus összefüggés használata elterjedt:
|
R [-] = 1 +ρs× Kd/ΘT |
(4.) |
ahol:
ρs= sűrűség (g/cm 3 ) és
ΘT= a víztelített víztartó réteg teljes porozitása (cm 3 /cm 3 ), vagy sok esetben a víztartó
víztartalmát használják föl, ami gyakorlatilag megegyezik a teljes porozitással.
Tehát ahhoz, hogy a megkötődő szerves vegyi anyagok terjedési sebessége (vc) számszerűsíthető legyen, a talajvíz szivárgási sebességét kell az R értékével elosztani:
|
vc[cm/s] = vx/R |
(5.) |
ahol:
vx [cm/s]= talajvíz szivárgási sebessége, melyet a következő képlet mutat be:
|
vx= k × i /ε |
(6.) |
ahol:
k = a víztartó hidraulikus vezetőképessége [cm/s],
i = horizontális hidraulikus gradiens [-]
ε = a vνztelített víztartó effektív porozitása [-].
A vegyületek szorpcióra való hajlama befolyásolhatja egyéb koncentrációcsökkentő folyamatok relatív fontosságát is. Pl. a párolgás sebessége a kémiai reakciók és a biodegradáció számos szerves vegyületnél direkt módon függ az adszorpció mértékétől.
| 5.3.2 Ionizáció, koszolvencia | |||
A szerves szennyezőanyagok szorpcióját, vagyis az oldott koncentrációt jelentősen befolyásolja a savas karakterű szennyezőanyagok – mint pl. a fenolok, kinolonok, krezolok, szerves savak – ionizációja, vagyis a pH-tól függő proton leadásuk, vagy felvételük. A képződött ionok nagyobb oldhatósággal jellemezhetők, mint a töltéssel nem rendelkező formáik, ezért az ionos formák Kocértékei is jóval alacsonyabbak. A vegyi anyag savi disszociációs állandója (pKa) alapján tehát meghatározható az a pH érték, ahol a Kocértéke lecsökken. pKaértéke azt a pH-t jelenti, ahol a molekulák 50%-a ionos állapotba kerül. Az ionos formák tehát kevéssé kötődnek a talaj szerves anyag tartalmához, viszont a töltéssel nem rendelkező formákkal szemben anionos adszorpcióval (lásd. 5.4.4 fejezet) oxidok felületén megkötődhetnek.
A megoszlási hányados savas karakterű szerves szennyezőanyagok esetén a következő:
|
Kd=Koc,n(1+10 pH-pKa ) -1 +Koc,i(1-(1+10 pH-pKa ) -1 ), |
(7.) |
ahol:
Koc,n= a nem ionizálódott vegyületforma szorpciós állandója (l/kg),
Koc,i= az ionizálódott vegyületforma szorpciós állandója (l/kg),
pKa = savi disszociációs állandó [-]
Gyakran feltételezik, hogy a felszín alatti vizek kémiai tulajdonsága az “abszolút” tiszta vízhez hasonló, és ezért a hidrofób szerves vegyi anyagok oldhatósága gyakorlatilag konstans egy szűk tartományon belül. Azonban ez gyakran téves feltételezés, mert elegyedő oldószerek keverékének jelenlétében, pl. víz-metanol elegyben – ha a metanol koncentráció nem is túl magas – a hidrofób szerves vegyi anyagok oldhatósága jelentősen megnőhet.
| 5.3.3 Abiotikus kémiai reakciók | |||
Az abiotikus kémiai reakciók olyan destruktív folyamatok, melyekben nem vesznek részt metabolikusan aktív szervezetek. Az ilyen reakciók leggyakoribb formái a hidrolízis, az elimináció, szubsztitúció és az oxidáció/redukció. A szénhidrogén szennyeződések (mint a BTEX) esetén az abiotikus reakciók nem számottevőek a felszín alatti környezetben, de több vegyi anyag esetében az abiotikus átalakulások eredményeképpen a szennyezőanyagok biodegradálhatósága megnövekedhet.
| 5.3.3.1 Hidrolízis | |||
A hidrolízis olyan nukleofil szubsztitúciós reakció, amelyben a szerves anyag reakcióba lép vízzel vagy hidroxid-ionnal, és alkoholt képez. A hidrolízises reakciók tipikusan elsőrendű reakciók. A hidrolízis sebessége szennyező anyagonként változik, a koncentráció-felezési idők pedig néhány naptól évekig terjedhetnek, mely egyértelműen jelzi az adott anyag hidrolízisre való hajlamát is. Hidrolízisre hajlamos szerves vegyületek a karbonsav-észterek, foszforsav-észterek, epoxidok, amidok, karbamátok, míg a hidrolízisnek ellenállnak az alkánok, alkének, aldehidek, benzol, PAH-ok, halogénezett aromás szénhidrogének, stb.
A hidrolízis sebességét erőteljesen befolyásolja a talajszemcsék felületén kialakuló pH különbség, a katalizátorként jelenlevő fémionok és az oldott szerves anyagok szorpció által történő megkötődése.
| 5.3.3.2 Szubsztitúció | |||
A hidrolízis is szubsztitúciós reakció - ahol két reagens helyettesítődési reakciójában bizonyos atomcsoportok melléktermékek keletkezése közben kicserélődnek – azonban ebben a reakcióban a víz van túlsúlyban, amely a szubsztitúciót előidézi. A felszín alatti környezetben azonban egyéb vegyi anyagok is előidézhetnek szubsztitúciót. Példaképpen megemlíthető, amikor a hidrogén-szullfid nukleofil szubsztitúciós reakcióban szerves anyaggal reagálva kéntartalmú szerves vegyületet hoz létre.
| 5.3.3.3 Elimináció | |||
Elimináció történik, amikor egy molekula kétfunkciós csoportot elveszít és helyettük kettős kötés alakul ki. Példaként említhető eliminációs reakcióra az 1,1-diklór-etilén (1,1-DCE) keletkezése 1,1,1-triklór etánból (1,1,1-TCA).
| 5.3.3.4 Oxidáció/redukció | |||
Redox reakció elektron-átmenetet jelent egyik komponenstől a másikig. Az oxidáció során a szerves vegyület elektront veszít, míg a redukció során elektronhoz jut. A legtöbb esetben, amikor egy szerves vegyi anyag redox átalakulása biológiai úton is végbemehet – és a feltételek adottak –, akkor az abiotikus reakciókkal szemben inkább a biológiai folyamatok válnak meghatározóvá.
| 5.4 Szervetlen vegyületek kémiai koncentrációcsökkentő folyamatai | |||
Az illékony szerves szennyezőanyagokat (VOC) követően a nehézfémek és a szervetlen szennyezőanyagok a leggyakoribb, a felszín alatti környezetet szennyező vegyi anyagok. A fémes szennyezőanyagok közül a leggyakoribbak az Ag, As, Ba, Cd, Cr, Ni, Hg, Pb, Se, Tl, Sb, Cu és Zn, míg a főbb egyéb szervetlen szennyezőanyagok közé tartozik a nitrát, foszfát, cianid és a radionukleidok. A vas, a mangán, az alumínium, a kalcium és a karbonát nem tartoznak a legfőbb szervetlen szennyezőanyagok közé, de a kármentesítések teljes költségéből jelentős hányadot képezhet az ezen szennyezőanyagok okozta lerakódások eltávolításának költsége (pl. sztrippeléses tisztítási technológiánál problémát jelent a karbonát- és Fe-kiválás). A szervetlen szennyezőanyagok viselkedését, felszín alatti környezetben való terjedését, kémiai formáját és toxicitását is jelentősen befolyásolják a fizikai és kémiai folyamatok. Ilyen folyamatok a kémiai speciáció, a beoldódás és kicsapódás, az oxidáció/redukció, az ioncsere és adszorpció a talajmátrixon, és a kolloidális méretű részecskékkel történő felszín alatti transzport. Az egyik nagy nehézség a szervetlen szennyezőanyagokkal kapcsolatban, hogy ezek a folyamatok gyakran egyszerre játszódnak le, ezért legtöbbször nehéz meghatározni, melyik a legfontosabb koncentrációcsökkentő folyamat. Ezeknek a folyamatoknak a relatív fontossága nemcsak területenként változik, hanem akár egy területen belül is eltérő lehet.
| 5.4.1 Kémiai speciáció | |||
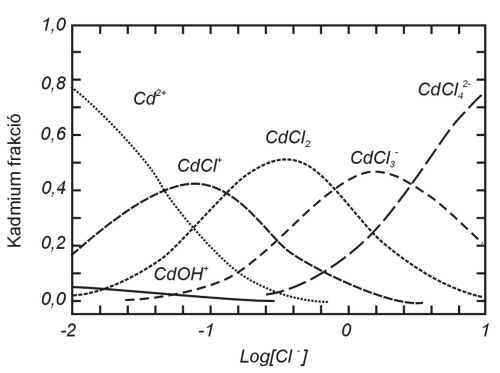
Amikor a vízmintát fémanalízis céljából bevisszük a laboratóriumba, az eredmény általában teljes (totál) fémkoncentráció formájában érkezik meg. A valóságban azonban a fémek a vízben jelen lévő anionokkal (vagy ligandumokkal) vannak kémiai kötésben és alakítanak ki különböző vegyületeket vagy komplexeket. Például a kadmium jelen lehet Cd 2+ , CdCl + , CdCl2, CdOH + formában is (5.4.1-1. ábra), vagy akár komplexet képezhet szulfáttal, karbonáttal, fluoriddal, szulfiddal, ammóniummal, foszfáttal, cianiddal vagy polifoszfáttal is. A komplexképzési hajlam az átmeneti fémeknél intenzívebb, mint más fémeknél. A relatív komplexképzési hajlam sorrendje a következő: Fe(III) > Hg > Cu > Pb > Ni > Zn > Cd > Fe(II) > Mn > Ca > Mg (Hanzlik, 1976). A komplexek koncentrációja függ a fémion koncentrációjától, a ligandum típusától és egyéb olyan jelenlévő ionok koncentrációjától, melyek versengenek a ligandumért.
5.4.1-1. ábra
Kadmium komplexek

Forrás: USEPA 1991.
A kémiai reakciók általában inkább a szabadion koncentrációtól függenek, mint a teljes fémkoncentrációtól, ezért a komplexek koncentrációjának ismerete fontos az olyan folyamatok pontos megismeréséhez, mint az adszorpció, az ásványok beoldódása és a kicsapódás. A szervetlen vizes komplexek kialakulása gyakran nagyon gyors, ezért egyensúlyi kifejezésekkel leírható. Pl. a higany-klorid komplex kialakulása (HgCl + ) leírható, mint egy egyszerű kémiai reakció:
|
Hg 2+ + Cl - = HgCl + , | <
(8.) |
melyre az egyensúlyi állandó felírható:
|
Ka= {Hg 2+ }{Cl - }/{HgCl + }, |
(9.) |
ahol a zárójelben szereplő kifejezések koncentrációt vagy aktivitást jelentenek. Az összes oldott állapotban jelenlévő kémiai forma (komplex) koncentrációjának kiszámításához ismernünk kell minden fém és minden ligandum koncentrációját, illetve minden egyensúlyi állandót. A fém és ligandum koncentrációk vízminták kémiai analízisével meghatározhatók, míg a szervetlen komplexekre vonatkozó egyensúlyi állandókat kutatási anyagokban és szakirodalomban lehet megtalálni. Bár ezeknek a komplexeknek a koncentrációját a fenti eljárás alapján könnyű kiszámítani, a fémeknek és a ligandumoknak igen kis számú kombinációja is nagy számú egyenletet (komplexet) eredményezhet. A kombinációkra vonatkozó számítások hosszú időt igényelnek és nehézkesek, de szerencsére már számos számítógépes program áll rendelkezésre, amelyekkel ezen számításokat könnyen és gyorsan el lehet végezni.
| 5.4.2 Beoldódás és kicsapódás | |||
A talajvíz a víztartóban való mozgása során az ásványi anyagok széles skálájával kerül közvetlen kapcsolatba. A talajvíz természetes kémiai összetételét tehát nagyban befolyásolja ezeknek az ásványoknak a mállása és beoldódása a vízbe. A beoldódás általában olyan reakciót jelent, melynek során az ásványokat alkotó vegyületek mindegyike oldatba megy. A sekély víztartóba beoldódó közönséges ásványok: a gipsz (CaSO4×2H2O), kalcit (CaCO3) és kvarc (SiO2). A mállás pedig egy részleges beoldódási folyamat, amelynek során bizonyos ionok oldatba mennek, mások pedig másodlagos ásványként maradnak vissza. Ha az oldatba került ionok koncentrációja eléggé magas, akkor ezek az ionok szilárd fázisként is eltávolíthatók az oldatból kicsapatással. A kicsapódott ásványok a víztartóban beállt kémiai és fizikai változások hatására később ismét oldott fázisba kerülhetnek.
Az ilyen típusú reakciók jelentősen befolyásolják a főbb oldott szennyezőanyag koncentrációkat is. Például kromáttal szennyezett talajvíz esetén BaCrO4válhat ki, mely később (a megváltozott körülmények hatására) ismét beoldódhat, ezzel megnyújtva a mentesítési időt. Továbbá az ásványok beoldódása során az eredetileg savas vagy bázisos jellegű víz semlegesítődhet, ezzel fokozva a fémek megkötődését és kicsapódását. A CaCO3vagy a Fe(III)-oxid kiválás csökkenti a víztartó áteresztőképességét, eltömi a kutak szűrőzését és növeli a tisztítási költségeket. A vizes és a szilárd fázisú anyag között beállt egyensúly – a komplex képződéshez hasonlóan – kifejezhető az egyensúlyi állandóval (Ksp), csak a reakció iránya fordított. A talajvíz oldó vagy kicsapató képességének leírására gyakran használják még a telítési indexet is:
SI = log (IAP/Ksp) (10.)
Az IAP számítása ugyanúgy történik, mint a Kspszámítása, csak a Ksp-vel szemben a nem egyensúlyi ion-koncentrációkat kell felhasználni a számításhoz. Tehát ha az adott vegyi anyagra nézve a víz és a szilárd fázis között egyensúly áll fenn, akkor az IAP = Ksp, és a telítési index = 0. Ha a telítési index < 0, akkor a víz telítetlen és a meglévőnél nagyobb mennyiségű anyagot képes oldani, ha pedig a telítési index > 0, akkor a víz túltelített, az oldott szilárd anyag kicsapódásra hajlamos. Az ásványi anyagokra vonatkozó telítési index számításához ismerni kell a vizes komplexek koncentrációját is, ezért az SI számítására a komplexeknél tárgyalt módszerek használhatók.
A telítési index jól használható a fémszennyezéssel érintett területek esetén a szennyező forrás azonosítására. Pl. ha a telítési index PbCO3-ra nézve közel van a nullához, akkor az ólom valószínűleg elkezdett kiválni az oldatból, és nem fog túl messze jutni a szennyező forrástól. Ha a vizes fázis és a szilárd fázis között telítetlen, illetve túltelített állapot becsülhető a telítési index alapján, akkor az IAP = Ksp (egyensúlyi állapot) figyelembe vételével kiszámolható az az 1 liter vízben feloldandó illetve kicsapatandó szilárd anyag mennyiség, amely az egyensúly eléréséhez szükséges. Az ilyen teoretikus számítás különösen hasznos lehet abban az esetben, amikor szennyezetett és szennyezetlen víz keveredésekor szeretnénk meghatározni a lehetséges ásványianyag beoldódást és kicsapódást.
| 5.4.3 Oxidáció/redukció | |||
Az elemek oxidációs számát a vegyértékhéjon lévő elektronok száma határozza meg, és az elemek többsége többféle oxidációs állapotban is előfordulhat. Az oxidációs-redukciós (redox) reakciók során elektronátadás történik, mely oxidációs szám változást eredményez. A redox reakciók tanulmányozása fontos a felszín alatti környezetbe került szennyezőanyagok viselkedésénél, mert az elemek kémiai tulajdonságai jelentősen megváltozhatnak az oxidációs szám változáskor. Például ha a felszín alatti gyengén savas környezet lúgossá válik, Fe(III)-hidroxid csapadék válik ki, és a kivált csapadék jelentős adszorpciós képességgel bír az egyéb oldott fémtartalomra nézve is. A vas (II) ezzel szemben oldékony, és oxidja jóval kisebb adszorpciós képességgel bír. Egy másik, környezetvédelmi szempontból fontos redox-aktív elem a króm. A hatos vegyértékű króm viszonylagosan mobilis, és toxikus anionos formában – HCrO4 - és CrO4 2- – van jelen a felszín alatti vizekben. A redukált állapotú króm Cr(III) pedig kationos formában van jelen, és gyengén savas és lúgos közegben is oldhatatlan, jól adszorbeálódik és sokkal kevéssé toxikus, mint a Cr(VI).
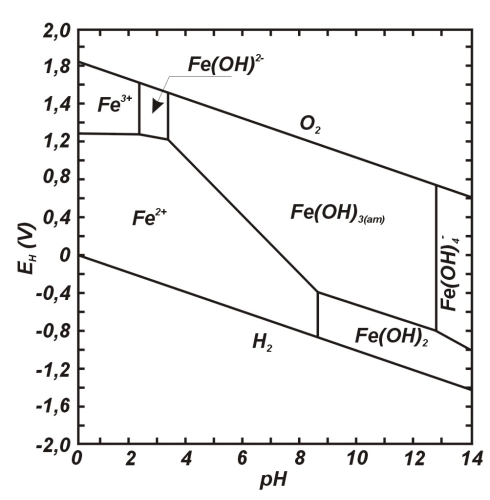
Egyensúlyi állapotban egy elem várható formáját a víz redox viszonyai és pH-ja határozza meg. A redox viszonyok a természetes vizekben az erősen oxidált (magas EH, +800-900 mV) állapottól egészen az erősen redukált (alacsony EH, -200 mV) állapotig változhatnak. Szennyezett vizekben a redox értékek legalább ezt a tartományt lefedik. Az adott pH-val és EH-val jellemezhető felszín alatti vízben teoretikusan stabilnak tekinthető vegyületformákat grafikusan EH-pH diagrammal (Pourbaix diagram) lehet szemléletesen bemutatni (5.4.3-1. ábra).
5.4.3-1. ábra
A vas EH-pH diagramja

Forrás: USEPA, 1991.
Például a vas EH-pH diagramja alapján látható, hogy magas redox érték mellett széles pH tartományban (gyengén savastól erősen lúgosig terjedően) a Fe(III)-hidroxid a domináns vegyületforma, míg alacsony redox érték mellett gyengén lúgos és savas körülmények között az oldott Fe(II) formák gyakoribbak. Tehát elméletileg az EH, pH értékek és a teljes fémkoncentráció ismerete lehetővé teszi az összes, talajvízben előforduló redox-aktív vegyületforma koncentrációjának mennyiségi becslését. Számos redox reakció azonban mikrobiológiailag katalizált vagy irreverzibilis, ezért egyensúlyi feltételekkel ezekben az esetekben nem lehet számolni.
| 5.4.4 Adszorpció, ioncsere | |||
Az oldott ionok koncentrációját a fenti folyamatokon túl jelentősen befolyásolhatja az ioncsere és az adszorpció koncentrációcsökkentő hatása is. A felszín alatti környezetben az agyagásványok rendelkeznek jelentős természetes ioncserélő képességgel. Az ioncsere folyamata során az agyagásványok felületén található kationok cserélődnek ki az oldatban lévő kationokra úgy, hogy közben az ásvány teljes töltése nem változik.
Például a Ca-Na ioncsere az alábbiak alapján írható le:
|
2NaX + Ca 2+ óCaX + 2Na + , |
(11.) |
és a Vanselow (1932) összefüggés segítségével közelíthető az ioncserét jellemző szelektivitási állandó:
|
Ks=(XCaX{Na + } 2 )/(X 2 NaX{Ca 2+ }, |
(12.) |
ahol NaX és CaX az agyagszemcsére szorbeálódott Ca és Na ionokat, míg az XNaX és XCaX a Na és Ca ionok által elfoglalt (kicserélhető) helyek molszázalékos arányát jelölik. A Ksmeghatározása empírikus összefüggésen alapszik, értéke erősen függ a vízben oldott ionkoncentrációtól, ezért helyspecifikus értékek használata szükséges a számítás során. Az ioncsere fontos koncentrációcsökkentő folyamat az alkáli- és alkáli földfémek esetében, míg az átmeneti fémek többségére inkább az adszorbciós folyamatok jellemzők. Az ionos adszorbció általában koordinációs kötések kialakulását jelenti a fém anionok/kationok és az ásványok felülete között. Az ioncsere során a szilárd fázis teljes elektrosztatikus töltése változatlan marad, míg az ionadszorpció során a felület töltése a pH-tól és a szorbeált ion mennyiségétől függően változik. Ezidáig nincs általánosan elfogadott módszer a szervetlen ionok adszorpciójának közelítésére.
Az oldott szerves anyagok adszorpciójához hasonlóan a szervetlen alkotók szorpciója is leírható adszorpciós izotermákkal. Általában az anionok adszorpciója a Langmuir-féle izotermát, míg a kationok szorpciója a Freundlich-féle izotermát követi (Dzombak, 1986).
|
Freundlich izoterma matematikai leírása: Kd=(C 1/N )/Cs |
(13.) |
|
Langmuir izoterma matematikai leírása: Kd=Cs/C(b-Cs) |
(14.) |
ahol:
C = a szennyezőanyag koncentrációja vizes fázisban [mg/l]
Cs = a szennyezőanyag koncentrációja szilárd fázishoz kötve [mg/kg]
b = a maximális megkötődő szennyezőanyag koncentráció [g/g]
N = vegyi anyag specifikus állandó (az 1/N értéke tipikusan 0,7-1,1-ig terjed)
A szervetlen vegyületek megkötődése erősen függ a talajvíz pH-jától, ezért a szervetlen ionok adszorpciója általában nem közelíthető a szerves vegyületeknél megszokott lineáris egyensúlyi adszorpcióval (5.4.4-1. ábra).
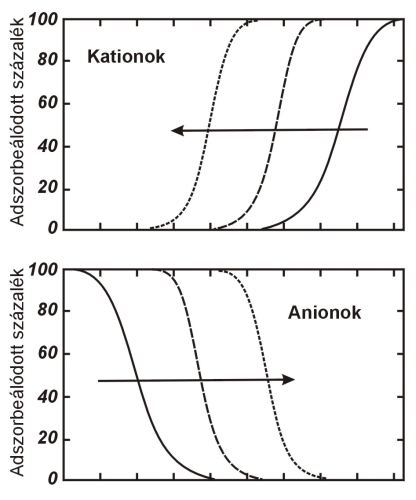
5.4.4-1. ábra
Adszorpciós izotermák

Forrás: USEPA, 1991.
Kationokból alacsony pH-n csekély mennyiség adszorbeálódik, míg a pH növekedésével a megkötött frakció aránya mindaddig nő, amíg adszorbeálható fémion van jelen, vagy az összes kötőhely be nem telik. A diagramon bemutatott pH-görbén elfoglalt pontos hely függ a fémkoncentrációtól, az adszorbens mennyiségétől és az egyéb jelenlévő oldott kationok koncentrációjától. Ez utóbbiak jelenlétében az adszorpciós helyek betöltődhetnek, vagy a vizsgált ionokkal komplexek képződhetnek, ezáltal a pH-görbe eltolódik. A pH-görbék lefutása az anionok esetében pontosan tükörképei a kationok görbéinek, vagyis maximális adszorpció tapasztalható alacsony pH-n, mely a pH növekedésével csökken.
| 5.4.5 Részecske transzport | |||
Szervetlen szennyezőanyagok transzportjában fontos szerepet játszik a részecskékkel történő terjedés. Ezek a kolloidális méretű részecskék lehetnek szervetlen, szerves vagy biológiai eredetűek, és tartalmazhatnak baktériumokat, vírusokat, természetes szerves anyagokat, szervetlen csapadékokat, azbesztet vagy egyéb ásványi agyagot is. A szervetlen ionok mozoghatnak a részecskék részeiként vagy a felületükhöz tapadva. A részecskék terjedésének távolságát nagyban befolyásolja a pórusokhoz viszonyított méretük. A lebegő részecskék három fő mechanizmus útján távolíthatók el a folyadék fázisból:
- kiszűrődés:ha a részecske mérete nagyobb, mint a víztartó legnagyobb pórusmérete, nem tud áthaladni a víztartón, ezért fennakad.
- derítés:ha a lebegő részecske kisebb, mint a legnagyobb pórusméret, de nagyobb, mint a legkisebb pórusméret, akkor valamennyi távolságot megtesz a víztartóban, mielőtt elérné azt a méretet, amelyen már nem tud áthaladni, és kiszűrődik.
- fizikai-kémiai folyamatok:ha a részecske mérete kisebb, mint a víztartó legkisebb pórusmérete, nagy távolságok megtételére képes, bár a részecskék a vizes fázisból homokszemcsékkel való ütközés és az azokhoz való hozzátapadás útján eltávolíthatók az oldatból. A homokszemcsékkel való ütközés kiülepedés és a Brown-mozgás következtében áll elő. A részecskék mérete meg is növekedhet (aggregáció), ha a kémiai körülmények, mint a pH vagy az ionerősség jelentősen változik. Az aggregálódott részecskék pedig derítéssel eltávolíthatók a vizes fázisból.
A kolloidális méretű részecskék terjedése nem minden felszín alatti környezetben jelentős tényező, ezért nagyon fontos meghatározni azokat a körülményeket, ahol ezen koncentráció csökkentő/növelő folyamatok számottevőek. Ilyen körülmények állnak elő abban a környezetben, ahol magas a szerves szén koncentráció, vagy az oldott vagy szuszpendált anyag mennyisége. A részecskék mozgása azokon a területeken jelentős, ahol a talajvíz áramlási sebessége nagy. Ha a felszín alatti környezet pH-jában vagy redox viszonyaiban hirtelen változás áll be, a kolloidális méretű csapadék-részecskéknek lehetősége van a víztartóban való mozgásra. Amikor a víz túltelített állapotban van, várható az egyensúlyi állapot kialakulása és a kicsapódott ásványi anyag részecske transzportja. Például oxigén jelenlétében közepesen savastól lúgos körülményekig magas vaskoncentráció mellett, a vas hajlamos finom kolloid méretű csapadék képzésére (vas-hidroxid). Ha a részecske transzport fontos folyamat, számos eljárás létezik annak kimutatására (szűrés, mikroszkópos eljárás, elektroforézis). Fontos elkülöníteni, hogy mit neveznek oldott állapotú anyagnak és mi tartozik a kolloidális mérettartományba. Több éven keresztül a 450 nm volt a választóvonal. A részecske transzport különösen azokon a területeken fontos, ahol a szennyezőanyag nagy toxicitású, és a nagy adszorpciós képessége miatt relatíve immobilis.
| 5.4.6 A szerves és szervetlen anyagok között fellépő hatások | |||
A szerves és szervetlen anyagok között fellépő hatások direkt és indirekt hatásokra oszthatók. A direkt hatások közé sorolható a fémionok szerves vegyületekkel történő komplexképzése (kelátképzés), redoxreakciók és a szerves-szervetlen vegyületek versengése az adszorpciós helyekért. Indirekt reakciók pedig a pH és a redox viszonyok megváltozása, melyek a szerves szennyezőanyagok bomlásának eredményeként következnek be. A direkt reakciók megismerésére vonatkozó kutatások többsége mesterséges viszonyokra vonatkozik, mint pl. az alkoholok oxidációja Cr(VI)-ion segítségével aldehiddé és karbonsavvá. Azonban ezek a kísérletek extrém koncentráció és pH viszonyok között zajlanak, tehát környezetvédelmi szempontból kis jelentőségűek. Néhány tanulmány azonban a szerves és szervetlen reakciók fontosságát hangsúlyozza, mint pl. a fenolok MnO2-dal történő oxidációja (Stone, 1986), szerves vegyületek fémmel szubsztituált agyaggal történő oxidációja (Voudrias és Reinhard,1986), vagy Cr(VI) krezolokkal történő redukciója (Fish és Elovitz, 1990). Még ha egy területen csak szerves szennyezőanyagok jelenléte várható is, a szervetlen komponenseket nem szabad figyelme kívül hagyni, mert a magas szervetlen ion koncentrációk – a direkt szennyezésen kívül – a természetesen előforduló ionok pH és redox körülmények változásának köszönhetően is képződhetnek. Ilyen változások gyakran állnak elő a szerves szennyezőanyagok biodegradációja során. A biodegradáció oxigént fogyaszt, ezért a redoxpotenciál értéke lecsökken a csóván belül. A biológiai bomlás eredményeként keletkező CO2és egyéb szerves savak pedig lecsökkentik a pH-t. Ez a folyamat eredményezi a vas(III)-oxid-hidroxid - mint fontos adszorbens - visszaoldódását és a fémionok deszorpcióját (újbóli visszaoldódását folyadék fázisba).
| 5.5 A szerves anyagok biológiai átalakulása | |||
A biológiai folyamatok destruktív koncentrációcsökkentő folyamatok. Számos tanulmány bizonyítja, hogy egy területen a honos mikróbák okozta biodegradáció jelentősen hozzájárulhat a szerves szennyezőanyagok lebontásához. Szénhidrogén szennyeződések esetében a - párolgás mellett - a biodegradáció az elsődleges természetes folyamat, ami a szennyezettséget csökkenti. A bidegradációs (destruktív) folyamatok lehetséges formáit az 5.1-1. táblázat mutatja be. A biodegradáció olyan elektron-transzfer folyamat, melyben a szervesanyagok táp- és energiaforrásként is hasznosulhatnak, az oxidációjukból nyert energia pedig a sejtek felépítéséhez és azok fennmaradásához járul hozzá.
A biodegradáció során lezajló elektron-transzfer és anyagcsere az alábbi generalizált egyenlettel írható le:
mikroorganizmusok + elektron donor + elektron akceptor + tápanyagokè
èanyagcseretermékek + energia + mikroorganizmusok
Alifás, illetve aromás szennyezőanyagok biodegradációja során maga a szennyezőanyag szolgál elektron donorként. Ilyen szennyezőanyagok esetén az aerob respiráció a leggyorsabb degradációs lépés, mely során a bontást aerob mikroorganizmusok végzik, és a végtermék CO2, H2O és biomassza. Fakultatív anaerob mikroorganizmusok képesek O2-t felhasználni elektron-akceptorként, ha az jelen van, vagy képesek alternatív elektron-akceptort is használni, illetve fermentálni is. Ilyen alternatív elektron-akceptorok a nitrát, szulfát, redukált vas, mangán; CO2és szerves anyag, melyek felhasználásra kerülnek, ha nincs jelen oxigén. Oxigén hiányában az obligát anaerobok kerülnek túlsúlyba. A biodegradáció sebessége anaerob körülmények között viszonylag lassú, a bomlástermékek egyszerű szerves savak, CO2, H2O, CH4, H2, N2és biomassza (sejtanyag). Néhány szerves szennyezőanyag, mint pl. a halogénezett szénhidrogének biodegradációja a fentieknél jóval bonyolultabb, (lásd az
5.1-1. táblázat: reduktív deklorináció, kometabolizmus).
A szennyezőanyagok biodegradációs hajlamát a felezési idő jelzi, mely akár egy vegyi anyagra vonatkozóan is meglehetősen nagy különbségeket mutathat (akár egy nagyságrend) helyszínről helyszínre. Még a relatív ellenálló vegyületek, mint az MTBE, PAH-ok és PCB-k is degradálódhatnak bizonyos környezeti feltételek mellett, míg előfordul, hogy a biodegradálhatónak tartott vegyi anyagok (pl. benzol) nem bomlanak. A degradáció sebességének (arányának) nagy változékonysága miatt gyakran nehéz a biodegradációnak betudható természetes koncentrációcsökkenés mértékének hosszú távú előrejelzése. Általában a biodegradálhatóság csökken a molekulatömeggel és/vagy az aromás gyűrűk számának növekedésével. Azonban például a halogénezett szénhidrogének reduktív deklorinációja során a nagyobb arányban klórozott vegyületek biodegradációja sokkal gyorsabban megy végbe, mint a kevésbé klórozott molekuláké. Szignifikáns bomlás csak akkor tapasztalható oldott fázisú vagy abszorbeált szerves vegyületek esetén, ha reziduális fázisú szennyezettség már nincs jelen. Általában az aerob bomlási folyamatok sokkal gyorsabbak mint az anaerob folyamatok, de gyakran az anaerob reakciók kritikusak a szennyezőanyag lebonthatósága szempontjából. A biodegradációs folyamatok a általában szennyezőanyag csóva egyes részein is különbözőek, mert az anaerob bontási folyamatok a csóva középpontjában, míg az aerob lebontás a csóva peremén folyik. Meg kell említeni, hogy a bomlás olyan közbülső melléktermékek keletkezéséhez is vezethet, melyek gyakran toxikusabbak/mobilisabbak mint a kiindulási vegyület.
| 5.6 A természetes koncentrációcsökkenés bizonyítékai | |||
A felszín alatti környezetbe kerülő főbb szennyező vegyi anyag – szerves és szervetlen – csoportok vizes fázisra vonatkozó koncentrációját csökkentő, vagy éppen növelő folyamatait a mért adatok segítségével meg kell jeleníteni (6. fejezet), illetve a térben és időben lezajló változásokat értelmezni és értékelni kell. Az értékelés célja annak meghatározása, hogy a koncentrációcsökkenés zajlik-e a területen és az milyen mértékű, illetve a tényfeltárás során meghatározott (D) kármentesítési szennyezettségi határérték a számított koncentráció-csökkenés mellett mikorra érhető el.
A koncentráció-csökkenés mértékét csak a bizonyítást követően van értelme számszerűsíteni.
Háromféle módon bizonyíható, hogy a vizsgált területen csökken-e természetes módon a szennyezőanyagok koncentrációja.
A természetes koncentráció-csökkenés egyértelmű (elsőrendű) bizonyítéka, ha a szennyezőanyag csóva csökkenő tendenciát mutat. A csökkenő csóva olyan jelenség, amelyben a szennyezettség határán (a talajvíz áramlási irányában a forrásterületnél kisebb talajvíz potenciálon lévő ponton), vagy egy csóván belüli ponton a kérdéses anyag koncentrációja lecsökken az idővel. Ez azt jelenti, hogy a természetes koncentráció-csökkenést előidéző folyamatok nagyobb mennyiségű szennyezőanyag lebontását képesek elvégezni, mint amekkora anyagmennyiség a forrásterületen belép a talajvíztérbe. Stabil csóva esetén a víztérbe belépő szennyezőanyag aránya megegyezik a koncentrációcsökkenés mértékével, míg növekvő csóva esetén a koncentráció-csökkenés mértéke kisebb, mint a belépő anyagmennyiség. Mind a természetes koncentráció-csökkenés, mind egy kármentesítés során – a csóva "életciklusa" – az oldott szerves szennyezőanyag csóvák többsége az összes fázison átesik (5.6-1. ábra).
5.6-1. ábra
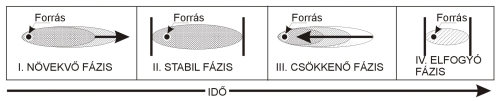
BTEX csóva elméleti életciklusa

Forrás: NEWELL R CONNOR, 1998.
A csóva stabilitásának becslése elvégezhető vizuálisan is, a szennyezőanyag koncentrációjának időben történő grafikus ábrázolásával az egyes mintavételi pontokra. A teljes szennyezőanyag csóva stabilitása, életciklus-helyzete pontosan megadható jól definiált statisztikai eljárásokkal, trendanalízissel (pl. lineáris regresszió vagy Mann-Kendall statisztika). A csóva stabilitását célzó statisztikai értékelésekhez legalább négy olyan monitoring kút és kutanként legalább négy olyan mintavételi kör eredménye szükséges, melyekben kimutatható koncentrációban jelen van a vizsgált szennyezőanyag. Azonban meg kell jegyezni, hogy már egyetlen (pl. a talajvíz áramlási irányában a forrástól legtávolabbi) ponton elvégzett trend-vizsgálattal becsülhető, hogy kialakulhat-e szennyezettség még szennyezetlen területeken a jövőben, és a kockázatfelmérésben felvett élőlény csoportok ténylegesen hatásviselők lesznek-e.
A nem paraméteres Mann-Kendall teszt használata széleskörben elterjedt a környezetföldtani gyakorlatban, mert alkalmas statisztika készítésére akkor is, amikor egy adatsor hiányos, az adatok eloszlása nem normál eloszlást követ, a mintavétel nem szabályos időközönként történt, vagy akár kimutatási határ alatti szennyezőanyag koncentrációkat is mértünk. Lineáris regresszió számításánál feltételezzük, hogy a rendelkezésünkre álló adatok normál eloszlást követnek. Ez ugyan elég szigorú megkötés, de amennyiben ez a mért adatokra vonatkozóan teljesül, a Mann-Kendall statisztikához képest ezzel a módszerrel pontosabb becslés adható a trendet illetően. Ezért célszerű mindkét eljárással elvégezni a trendanalízist minden vizsgált pontra és szennyezőanyagra, ha nagy mennyiségű adat áll rendelkezésre egy szennyezett területen. A szennyező forrás területén, valamint a csóva egyéb részein található kutakra kiszámított trendek ismeretében megállapítható, hogy a csóva életciklusának melyik részében jár, vagyis növekvő, stabil vagy csökkenő fázisban van-e. A kármentesítés során elérendő mentesítési célértékek és a változások ütemének (csóvadinamika) ismeretében az is megállapítható, hogy az egyes mintavételi pontokon alkalmazott mintavételi gyakoriság megfelelő-e, vagy ritkábban, esetleg gyakrabban kell mintázni.
A természetes koncentráció-csökkenés másodrendű bizonyítása a kémiai és bio(geo)kémiai indikátorok koncentrációjában beállt változások mérése útján lehetséges.
Erre két módszer szokásos:
- A kémiai és geokémiai analitikai adatokat felhasználva tömeg-mérleget kell készíteni, és ennek segítségével kell bemutatni, hogy a vizsgált szennyezőanyag koncentráció csökkenése, és/vagy az elektron donor/akceptor koncentráció csökkenése közvetlen összefüggést mutat-e a metabolikus anyagcseretermékek és/vagy az anyagcseretermékek koncentrációjának növekedésével.
- A monitoring tevékenységből származó kémiai adatok felhasználásával "tracer"-tesztet kell elvégezni. Ezen eljárás során a biodegradációnak ellenálló nyomjelző anyag segítségével kerül meghatározásra, hogy a szennyezőanyag csóva stabil-e, vagy a csökkenés, illetve növekedés sebessége hogyan viszonyul a konzervatív módon – a destruktív koncentrációcsökkentő folyamatok elhagyásával – számolt víz terjedési sebességhez.
A csóva stabilitásra, illetve a lecsökkent szennyezőanyag mennyiségre vonatkozó értékelést grafikus ábrázolást követően akár vizuálisan is el lehet végezni, de statisztikai eljárások (Mann-Whitney és Mann-Kendall) is használatosak a kiértékelésre.
A természetes koncentráció-csökkenés harmadrendű, vagy opcionális bizonyítékai azok a laboratóriumi mikrobiológiai vizsgálatok, melyek az adott felszín alatti környezetben élő honos mikroorganizmusok bontási képességét. A mikrobiális lebontóképességet általában csak akkor vizsgálják, ha az első és másodrendű bizonyítékok vizsgálata nem vezetett eredményre.
Az analitikus és numerikus szennyeződés-terjedési modellek kiegészíthetik a bizonyítékok sorát azáltal, hogy:
- bemutatják a különbségeket a mért és az előrejelzett szennyezőanyag koncentrációk között,
- segítségükkel megbecsülhető a különböző koncentrációcsökkentő folyamatok egymáshoz viszonyított fontossága.
| 5.7 A természetes koncentrációcsökkenés monitoringjához szükséges minimális adatigény, vizsgálandó paraméterek | |||
Annak érdekében, hogy a monitoring vizsgálatok alapján értékelhetők legyenek a felszín alatti környezetben zajló folyamatok, meg kell határozni a vizsgálandó paraméterek körét. A vizsgálandó paraméterek körét meghatározzák a szennyezőanyagok tulajdonságai, a domináns koncentrációcsökkentő folyamatok és az adott területre jellemző “biogeokémiai” környezet is. A koncentrációcsökkentő folyamatok értékeléséhez szükséges fizikai, kémiai, biológiai, geológiai-hidrogeológiai és geokémiai paraméterek listáját a 5.7-1. táblázat mutatja be összefoglalóan. A táblázat leírja azokat az adatokat, melyek egy egyszerű hidrogeológiai és terjedési modell építéséhez szükségesek, valamint a természetes koncentrációcsökkenés bizonyítását (első-, másod- illetve harmadrendű bizonyítékok) lehetővé teszik.
5.7-1. táblázat
Adatigény a természetes koncentrációcsökkenés megítéléséhez és értékeléséhez
|
Kulcs-paraméterek a becsléshez |
Alkalmazhatóság |
Használat + |
Használhatóság a természetes koncentrációcsökkenés megítéléséhez | ||
|
Általában |
Szerves vegyi anyagokra |
Szervetlen vegyi anyagokra | |||
|
A. Geológiai és hidrogeológiai | |||||
|
Kőzettan |
X |
EM |
Megmutatja a víztartó olyan izotróp jellemzőit, mint a preferált áramlási útvonalakat, víztartó és vízzáró egységeket. Kijelöli a talajvíz áramlási irányát és utal az áramlási sebességre. | ||
|
Porozitás |
X |
EM; V&T |
Kulcsfontosságú a talajvíz terjedésében. | ||
|
A víztartó réteg vezető-képessége |
X |
EM; V&T |
Nélkülözhetetlen a szennyezőanyag csóvák tanulmányozásakor. | ||
|
Évszakos vízszint fluktuáció |
X |
EM |
Meghatározza szennyezett zóna kiterjedését, a felszín alatti víz évszakonkénti sebesség- és irányváltozását. | ||
|
Utánpótlás mértéke |
X |
EM |
A felszín alatti víz mozgásának egyik alapvető tényezője.
| ||
|
B. Kémiai | |||||
|
Kiindulási szennyezőanyag és bomlástermék koncentrációk |
X |
I |
Felhasználható a biodegradáció kinetikájának leírására, mint például felezési idő vagy a degradációs sebesség becslésére. | ||
|
Egyéb jelenlévő szennyezőanyag koncentrációja |
X |
X |
I |
Kometabolitként vagy katalizátorként viselkedő szennyezőanyagok olyan termodinamikailag kedvező folyamatok jelenlétére is utalhatnak, mint a biodegradáció kometabolizmussal. | |
|
C. Geokémiai | |||||
|
Oldott oxigén |
X |
X |
II |
Szerves vegyi anyagok biodegradációja során az energetikailag legkedvezőbb folyamat az oldott oxigén redukciója, az oldott oxigén a legtöbb energiát adó elektron akceptor. A kisebb, mint 0.5 mg/l DO koncentráció általában anaerob biodegradációra utal. | |
|
Nitrát |
X |
X |
II |
Az oxigén után a legkedvezőbb elektron akceptor termodinamikai szempontból szerves anyagok mikrobiológiai degradációjánál. A csökkenő nitrát koncentráció anaerob (denitrifikáció) degradációt jelezhet. | |
|
Nitrit |
X |
II |
A nitrát redukálódásának terméke. Csak anaerob körülmények mellett keletkezik. Ritkán megfigyelt. | ||
|
Vas (III) |
X |
II |
A biológiailag elérhető vas (III) viselkedhet elektron akceptorként szerves anyagok anaerob biodegradációja közben. | ||
|
Vas (II) |
X |
II |
Jelzi a vas (III) redukciót szerves vegyületek mikrobiológiai degradációja közben, oxigén, nitrát és mangán (IV) hiányában. | ||
|
Mangán (IV) |
X |
II |
Viselkedhet elektron akceptorként olyan anaerob biodegradációs folyamatokban, ahol termodinamikailag kedvezőbb elektron akceptorok nincsenek jelen. | ||
|
Mangán (II) |
X |
II |
Olyan szerves anyagokat degradáló anaerob folyamat jelzője, ahol a mangán (IV) elektron akceptorként viselkedik. | ||
|
Szulfát |
X |
X |
II |
Szerves anyagok biodegradálódásánál mint elektron akceptor használódik fel. Redukciós terméke a szulfid. | |
|
Szulfid |
II |
Mikrobiológiai úton redukált formája a szulfátnak. Redukált körülményeket jelez. | |||
|
Metán |
X |
II |
Az anaerob körülmények és a szerves anyag metanogén baktériumok általi biodegradációjának jellemzője. Szén-dioxidból keletkezik biológiai redukcióval. | ||
|
Etán és etén |
X |
Klórozott oldószerek biológiai átalakulásának kimutatására szolgál. | |||
|
Oldott hidrogén |
II |
A redox környezet indikátora, mivel a koncentrációja összefüggésben van az anaerob mikrobiológiai aktivitásokkal (metanogenezis, szulfát redukció). | |||
|
Teljes szerves széntartalom |
X |
II |
A szerves anyag koncentráció mérőszáma (természetes és antropogén) vízben, ami a biodegradáció elsődleges szubsztrátjaként viselkedhet. (reduktív dehalogenezáció) | ||
|
pH |
X |
X |
II |
A mikrobiológiai aktivitás korlátozott a pH 6-8.5 terjedő sávon kívül, és sok anaerob baktérium különösen érzékeny a szélsőséges pH-ra. A fémek felszín alatti környezetben való viselkedése erősen pH-függő. | |
|
Lúgosság/teljes szervetlen szén tartalom (TIC) |
X |
X |
II |
A víz puffer kapacitásáról és a benne oldott szén-dioxid mennyiségéről tanúskodik. Az oldott CO2tartalom növekszik a szerves anyagok biodegradációja során. | |
|
pe/Eh (redox potenciál) |
X |
X |
II |
A felszín alatti környezet oxidatív/reduktív potenciáljának mérőszáma. Tartománya általában +800mV-tól tart (erősen aerob körülmények) –400mV-ig. (metanogén állapot) | |
|
Hőmérséklet |
X |
X |
II |
A mikrobák metabolizmusát befolyásolja. Alacsonyabb hőmérsékleten lassabb a biodegradáció sebessége. Befolyásolja a redox folyamatokban résztvevő szennyezőanyagok oldhatóságát. | |
|
Klorid |
X |
II |
A biológiai deklorináció (“klórtalanítás”) jelzője lehet. Konzervatív nyomjelző anyagnak használják. | ||
|
Vezetőképesség |
X |
II |
Általános vízminőség jellemző, amit arra használnak, hogy megbizonyosodjanak a vízminták azonos víztartó rétegbeli származásáról. | ||
|
Foszfor |
X |
II |
Nélkülözhetetlen tápanyag a mikroorganizmusok fejlődéséhez és a biodegradációhoz. | ||
|
Etán/etilén |
X |
II |
A halogénezett etilén és etán reduktív dehalogenizációja során keletkezett metabolikus végtermék. Metanogén mikrobiális aktivitást jelezhet. | ||
|
Illékony zsírsavak |
X |
II |
A BTEX aerob degradációjának metabolikus végterméke. | ||
|
Dehidrogenáz |
X |
III |
Aerob baktériumok jelenlétére utal. | ||
|
Szén-dioxid |
X |
II |
Szerves anyagok metanogén (anaerob) degradációjában elektron akceptorként viselkedik, ugyanakkor sok szerves anyag biodegradációjának végterméke. | ||
|
D. Biológiai | |||||
|
Mikroba szám/biomassza |
X |
III |
Jelzi, hogy az őshonos mikróbák képesek-e lebontani a szennyezőanyagot, és információval szolgáltat a degradáció mértékéről. | ||
|
RNS próbák |
X |
III |
A szennyezőanyagot bontó specifikus baktériumok kimutatására szolgál. | ||
Megjegyzés az 5.7-1. táblázathoz:
+ EM = elméleti modellépítéshez szükséges
V&T = a felszín alatti környezetben való viselkedés és terjedés modellezéséhez szükséges
I;II;III; = a természetes koncentráció-csökkenés első-, másod- és harmadrendű bizonyítékai
Az 5.7-2. táblázat az egyes koncentráció-csökkentő folyamatok bemutatásához szükséges paraméterek körét mutatja be, míg az 5.7-3. táblázat a leggyakrabban előforduló szennyezőanyagok koncentráció-csökkenésének nyomon követésére szolgáló vizsgálandó paraméterek körére és rendjére mutat be példát.
5.7-2. táblázat
A főbb koncentráció-csökkentő folyamatok igazolását szolgáló paraméterek
|
Koncentráció-csökkentő mechanizmus |
Áramlási viszonyok a víztartóban |
Kémiai tulajdonságok |
Cél szennyezőanyag koncentráció |
Egyéb jelenlévő szennyezőanyag koncentáció 1 |
Bomlástermék koncentráció |
Oldott oxigén |
Teljes szerves széntartalom (TOC) |
Elektron akceptorok koncentrációja 2 |
Redox |
pH |
Lúgosság |
Hőmérséklet |
Klorid |
Hozzáférhető vas hidroxid |
Hidrogén |
|
Higulás, diszperzió és diffúzió |
xx |
xx |
xx |
x | |||||||||||
|
Szorpció és kicsapódás |
xx |
xx |
xx |
x |
xx |
xx |
xx |
x |
xx | ||||||
|
Párolgás |
xx |
x |
x | ||||||||||||
|
Aerob degradáció (a szennyezőanyag mint elektron donor) |
xx |
xx |
xx |
x |
x |
x |
x |
x |
x |
x |
x |
x | |||
|
Anaerob degradáció (a szennyezőanyag mint elektron akceptor) |
xx |
xx |
xx |
x |
x |
x |
x |
x |
x |
x |
x |
x |
x | ||
|
Reduktív dehalogenezáció (a szennyezőanyag mint elektron akceptor) |
xx |
xx |
xx |
xx |
xx |
xx |
xx |
xx |
xx |
xx |
x |
x |
x |
x |
xx = alapvetően fontos vizsgálni,
x = ajánlott vizsgálni
1: pl. petróleum szénhidrogének vagy klórozott szénhidrogének
2: pl. Fe 3+ , Mn 4+ , NO3 - , SO4 2- , CO2(elektron akceptorok) és Fe 2+ , Mn 2+ , NO2 - és N2, H2S, CH4(mint metabolikus anyagcseretermékek)
5.7-3. táblázat
Koncentráció-csökkenési folyamatokat nyomon követő analitikai vizsgálatok
|
Szennyezőanyag |
Kezdeti mintavétel |
Későbbi mintavétel(1) |
|
BTEX, fenol | ||
|
Csóván belül |
BTEX/fenol, DO, NO3, Fe(II), SO4, CH4, CO2, lúgosság, vízszint, NAPL vastagsága |
BTEX/fenol, vízszint |
|
Csóván kívül (3) |
BTEX/fenol, DO, NO3, Fe(II), SO4,CH4, CO2, lúgosság, vízszint(2) |
BTEX/fenol, vízszint |
|
Klórozott oldószerek | ||
|
Csóván belül |
Klórozott komponens +bomlástermékek, TOC, DO, NO3, Fe(II), SO4, CH4, Cl, vízszint, NAPL jelenlét |
Klórozott komponens + bomlástermékek, Cl, vízszint |
|
Csóván kívül (3) |
Klórozott komponens + bomlástermékek, TOC, DO, NO3, Fe(II), SO4, CH4, Cl, vízszint |
Klórozott komponens + bomlástermékek, Cl, vízszint |
|
Fémek | ||
|
Csóván belül |
Fém, redox, DO, vízszint |
Fém, vízszint |
|
Csóván kívül (3) |
Fém, redox, DO, vízszint |
Fém, vízszint |
|
Ammónia | ||
|
Csóván belül |
Ammónia, nitrát, vízszint, pH |
Ammónia, vízszint |
|
Csóván kívül (3) |
Ammónia, nitrát, vízszint, pH |
Ammónia, vízszint |
|
MTBE | ||
|
Csóván belül |
MTBE + bomlástermékek, DO, NO3, Fe(II), SO4, CH4, CO2, lúgosság, vízszint |
MTBE, vízszint |
|
Csóván kívül (3) |
MTBE + bomlástermékek, DO, NO3, Fe(II), SO4, CH4, CO2, lúgosság, vízszint |
MTBE, vízszint |
- A kiindulási szennyezőanyag koncentráció és a vízszint csak példák olyan paraméterekre, amelyeket rendszeresen mérni kell, azonban elképzelhető, hogy egyéb paramétereket (pl. DO, NO3, SO4) is rendszeresen monitoringozni kell.
- A pontos biogeokémiai paramétereket a biodegradációs folyamat alapján kell meghatározni.
- A csóván kívül, beleértve a szennyezetlen – nagyobb vízpotenciálon lévő “upgradient”– háttér monitoring ponto(ka)t is.
| 5.8 A természetes koncentráció-csökkenés számszerűsítése | |||
Számos módszer létezik a természetes koncentráció-csökkenés, illetve a biodegradáció mértékének meghatározására. A természetes koncentráció-csökkenés mértékének számszerűsítése megerősíti a leíró, vagy fél-kvantitatív vizsgálati eredményeket. A monitoring tevékenység során az alábbi módszerek valamelyikével minden vizsgálati periódusban megbecsülhető a természetes koncentráció-csökkenés, illetve a biodegradáció mértéke, melyek ismeretében becsülhető a kívánt szennyezettségi szint elérésének ideje. A monitoring vizsgálati eredmények ismeretében pedig eldönthető, hogy az alkalmazott becslési módszer megfelelő-e az adott területre. A lehetséges módszerek közül a négy gyakran használt eljárás leírása az alábbi:
1. A tömegegyensúly (tömegmérleg) módszere:
A természetes koncentráció-csökkenés értéke megbecsülhető a szennyező forrásból a talajvíztérbe jutó szennyezőanyag mennyiségének számításával stabil vagy csökkenő csóvák esetén. Stabil csóva esetén a talajvíztérbe jutó szennyezőanyag mennyisége megegyezik a természetes koncentráció-csökkenés mértékével, hiszen a csóva peremén nem növekszik és nem csökken a koncentráció. Míg csökkenő csóva esetén a természetes koncentráció-csökkenés miatt az elfogyó szennyezőanyag mennyisége a csóván belül nagyobb, mint a talajvíztérbe jutó szennyezőanyag mennyisége. Ebből látható, hogy a talajvíztérbe egységnyi idő alatt belépő oldott szennyezőanyag mennyisége adja a természetes koncentráció-csökkenés értékét stabil csóva esetén.
2. Grafikus és regressziós technikák:
Az szennyezőanyag oldott koncentrációja idővel és távolsággal történő változása a természetes koncentráció-csökkentő folyamatok eredménye. A természetes koncentráció-csökkenés grafikus ábrázolása szerint:
- A csóva középvonalában a szennyezőanyag koncentrációját a távolság függvényében kell ábrázolni (log-lineáris diagram) egy adott időpillanatban. Ez az eljárás csak stabil és csökkenő trendet mutató oldott szennyezőanyag csóvák esetén alkalmazható. Elsőrendű bomlás esetén a log-lineáris diagramban az összefüggés egyenessel közelíthető.
- A csóván belül egy ponton a szennyezőanyag koncentrációjának időbeli változását kell ábrázolni. A koncentráció és az idő összefüggése itt is egyenessel írható le, de ez a módszer csak csökkenő csóvára alkalmazható.
Mindkét esetben a pontokra illesztett egyenes meredeksége fogja megadni a természetes koncentráció-csökkenés mértékét. A biodegradációnak köszönhető rész a szennyezőanyag koncentráció és egy konzervatív nyomjelző anyag a koncentráció áramlási pálya mentén történő összehasonlításával adható meg. “Tracer”-teszt során olyan vegyi anyagot kell alkalmazni, amely a biodegradációnak ellenáll, hasonló Henry-állandóval és szorpciós tulajdonságokkal rendelkezik, mint a vizsgálni kívánt szennyezőanyag.
3. Terjedési modellek alkalmazása:
A tömegegyensúly- és grafikus/regressziós technikák nem tesznek különbséget a szorpció, a diszperzió és a biodegradáció között, szemben a terjedési modellekkel, ahol a biodegradációnak a teljes koncentráció-csökkenéshez való viszonya is vizsgálható. A koncentráció távolsággal történő regresszióját stabil csóvára egydimenziós analitikus “steady-state” megoldással kombinálta Buscheck és Alcantar. Az állandósult transzport folyamatokra vonatkozó analitikus megoldás egyenlet segítségével becsülhető egy csóva adott időbeli kiterjedése és az elsőrendű bomlási állandó értéke (Domenico).
4. Elektron egyensúlyszámítás:
Az elektron egyensúlyszámítás felhasználható egy víztartóban a szennyezést-lebontó képesség (asszimilációs kapacitás) becslésére. Az eljárás alapja: a vizsgált terület különböző részein a talajvíz kémiai tulajdonságaiban mért változások és az oxidációs/redukciós reakciók során lebomlott szennyezőanyag és anyagcseretermék mennyiség sztöchiometrikus leírása. A mikrobális anyagcsere folyamatok nyomon követésével azonosítható az eltérő mikrobális aktivitás területi eloszlása. A biodegradációs vagy asszimilációs kapacitás tehát az a szennyezőanyag koncentráció, amelyet a mikroorganizmusok a víztartó elektron akceptorai segítségével képesek lebontani.